- 029-86354885
- 18392009562
現(xiàn)化療被認為是治療癌癥的主要選擇之一,而癌癥仍是全球醫(yī)療保健最普遍致命的疾病之一。絲裂霉素C(MMC)是種有效的水溶性化療藥物,同時MMC是P-糖蛋白的不良底物,并且保留了對許多類型的P-糖蛋白介導(dǎo)的多藥抗性癌細胞的活性。但缺陷眾多,如水穩(wěn)定性差,非特異性生物分布,血漿快速消除,嚴重的全身毒性和狹窄的治療窗口。
藥物-磷脂復(fù)合物技術(shù)比以往更加引起研究人員對新型藥物制劑的關(guān)注,在保持藥物的藥理作用的同時顯示出提高藥物安全性,生物利用度和功效的巨大優(yōu)勢。磷脂具有高度疏水性和超嗜好性,使其成為藥物輸送系統(tǒng)核心結(jié)構(gòu)的有吸引力的選擇。因此,將藥物-磷脂復(fù)合物引入常規(guī)藥物遞送系統(tǒng)(例如脂質(zhì)或基于聚合物的NPs)可能提供新的藥物遞送方法。
1,2-二硬脂酰基-sn-甘油-3-磷酸乙醇胺-N- [甲氧基(聚乙二醇)-2000](DSPE-PEG),一種廣泛使用的磷酸乙醇胺 - 聚乙二醇(PEPEG,也是市售的磷脂,含有PEG spacer)是一種有吸引力的兩親脂質(zhì) - 聚合物綴合物,包括親水性PEG和極度疏水的脂肪酸,并已通過FDA認證用于臨床應(yīng)用。此外,PEG-脂質(zhì)結(jié)合物DSPE-PEG不僅廣泛用于抗癌藥物遞送的自組裝關(guān)鍵材料,而且還用作表面功能化各種藥物遞送系統(tǒng)的添加劑材料。由脂質(zhì),聚合物,無機材料,甚至那些材料的雜合組合組成,導(dǎo)致體外和體內(nèi)穩(wěn)定性和藥代動力學(xué)的改善,這是PEG化誘導(dǎo)的免疫原性降低的結(jié)果。
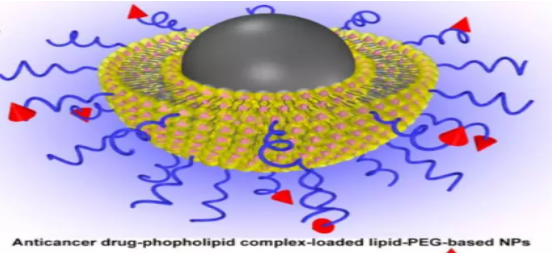
綜合絲裂霉素C(MMC)- 磷脂復(fù)合物提高藥物包封率和減少過早藥物釋放,以及DSPE-PEG-葉酸(DSPE-PEG-FA)用于特定腫瘤靶向的優(yōu)勢,報道了一種簡單的一鍋自組裝途徑制備負載MMC-磷脂復(fù)合物的基于DSPE-PEG-FA的納米顆粒(MP-PEG-FA NPs)。共聚焦成像和流式細胞術(shù)均證明MMC在細胞攝取和細胞內(nèi)藥物遞送后分布到細胞核中。更重要的是,全身施用MP-PEG-FA NPs后導(dǎo)致在攜帶HeLa腫瘤的裸鼠中血液持久性增加和腫瘤累積增加。研究介紹一種簡單有效的策略,基于抗癌藥物-磷脂復(fù)合物的靶向給藥系統(tǒng),用于持續(xù)/控制藥物釋放。
將藥物-磷脂復(fù)合物(或親水性藥物-磷脂復(fù)合物)引入聚乙二醇化脂質(zhì)的藥物遞送系統(tǒng)中,以增加藥物負載能力和改善癌癥治療的藥物遞送功效。
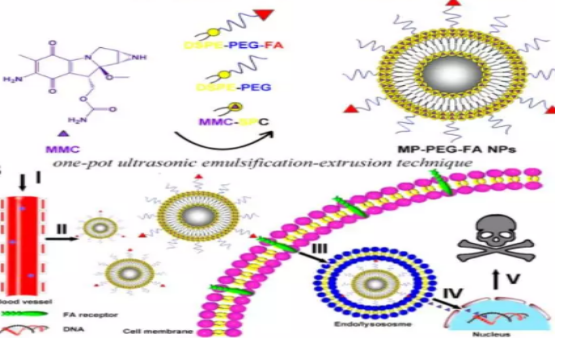
通過將抗癌藥物-磷脂復(fù)合物引入基于脂質(zhì)-PEG的自組裝藥物遞送系統(tǒng),可以將水溶性MMC藥物加載到MP-PEG-FA NPs中以延長藥物保留在血液循環(huán),并允許主動靶向特定組織和在所需疾病部位的雙重可控藥物釋放。這種簡單,有效和靈活的策略提供了一種有前景的靶向控制癌癥的治療藥物輸送系統(tǒng),并將有助于其他基于抗癌藥物-磷脂復(fù)合物的自組裝藥物輸送系統(tǒng)。
| 序號 | 新聞標題 | 瀏覽次數(shù) | 作者 | 發(fā)布時間 |
|---|---|---|---|---|
| 1 | 抗氧化小分子70831-56-0,菊苣酸Cichoric Acid,6537-80-0的制備過程 | 862 | 瑞禧生物 | 2023-03-30 |
| 2 | 活性氧ROS小分子Dapsone,cas:80-08-0,氨苯砜的制備過程-瑞禧科研 | 766 | 瑞禧生物 | 2023-03-30 |
| 3 | HBPS-N3,Azide-PEG-HBPS,疊氮化超支化聚苯乙烯高分子聚合物的制備過程 | 892 | 瑞禧生物 | 2023-03-17 |
| 4 | l-PS-PhN3,Azide疊氮Azido偶聯(lián)線性聚苯乙烯雙鏈的制備過程 | 814 | 瑞禧生物 | 2023-03-17 |
| 5 | N3-PS-N3,Azido-PS-Azido/Azide,雙疊氮官能團修飾聚苯乙烯的制備方法 | 773 | 瑞禧生物 | 2023-03-17 |
| 6 | PS-N3,Azido-PS,疊氮Azide修飾聚苯乙烯/高分子聚合物的制備過程 | 961 | 瑞禧生物 | 2023-03-17 |
| 7 | Azido-PEG2-t-Butylester/1271728-79-0,疊氮N3/ZAD修飾叔丁酯化合物的制備方法 | 795 | 瑞禧生物 | 2023-03-14 |


 400-115-0588
400-115-0588 在線咨詢
在線咨詢







 庫存查詢
庫存查詢